Criptosporidiosis en terneras: el secreto está en el ciclo I
DICIEMBRE 2024 | RECRÍA
Cryptosporidium parvum es uno de los principales patógenos causantes de la diarrea en las terneras lactantes. En este estudio analizamos el “secreto de su éxito” para su expansión en la granja, enumeramos los factores de riesgo y ofrecemos algunos puntos de manejo clave para minimizar la presión de infección y maximizar su inmunidad en las primeras semanas de vida de nuestros animales.
INTRODUCCIÓN
La diarrea neonatal es una enfermedad multifactorial compleja y constituye la principal causa de problemas de salud y mortalidad en terneras lactantes. Tanto ganaderos como veterinarios están familiarizados con las pérdidas económicas asociadas a las bajas de terneras, las visitas veterinarias, los tratamientos y el tiempo de mano de obra. En cambio, no existe tanta consciencia sobre las repercusiones que causa la diarrea tanto a corto plazo, con una menor ganancia de peso y mayor riesgo de sufrir neumonía posterior, como a largo plazo, debido al retraso reproductivo y la menor producción de leche en primera lactación (Abuelo et al., 2021; Schinwald et al., 2022).
Entre las principales causas infecciosas de diarrea, nos encontramos con virus, bacterias y parásitos. Los agentes más frecuentemente involucrados son Escherichia coli (E. coli), rotavirus, coronavirus y Cryptosporidium parvum (Cho & Yoon, 2014). Estos patógenos pueden actuar tanto de manera aislada como en infecciones mixtas, en las que se incrementa la gravedad clínica y amplía el rango de edad de los animales afectados. Por ello, establecer un diagnóstico adecuado será clave a la hora de decidir las medidas de prevención más efectivas.
Dentro del género Cryptosporidium se incluyen al menos 44 especies de protozoos gastrointestinales que pueden afectar a numerosos mamíferos, incluido el hombre (Chalmers et al., 2019). En el caso de los terneros, C. parvum es la principal especie causante de diarrea, especialmente a los terneros entre la segunda y tercera semana de vida (Shaw et al., 2021), con una amplia distribución mundial y presencia en los rebaños lecheros (Santin, 2020).
¿Y por qué tiene este parásito una distribución tan amplia? ¿Cuál es el secreto de su éxito?
El ciclo comienza cuando los bovinos ingieren las formas de resistencia del protozoo, que se denominan ooquistes, presentes en alimentos, agua o medio ambiente
EL SECRETO ESTÁ EN EL CICLO
En primer lugar, es necesario conocer las diferentes etapas del ciclo del parásito, lo que nos aportará las claves de su éxito. Cryptosporidium parvum presenta un ciclo directo (imagen 1), es decir, necesita un único animal para completarlo.
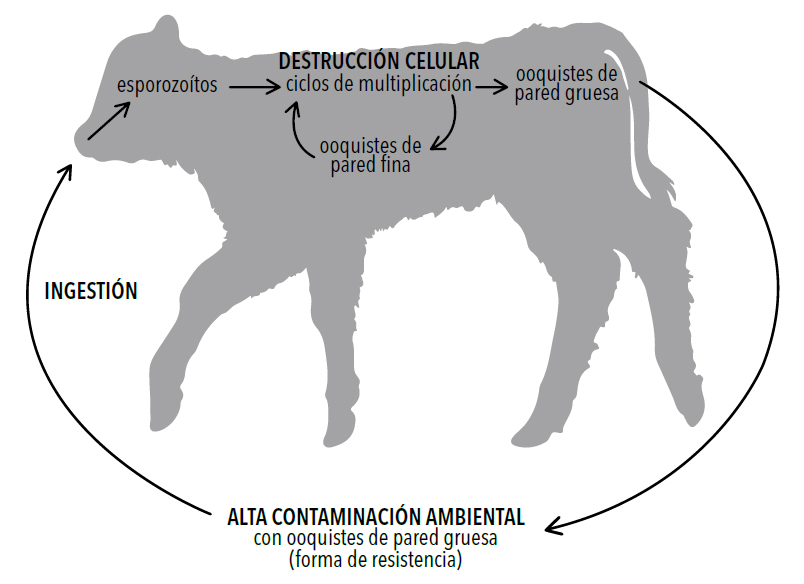
Imagen 1. Ciclo del parásito
El ciclo comienza cuando los bovinos ingieren las formas de resistencia del protozoo, que se denominan ooquistes, presentes en alimentos, agua o medio ambiente. Los ooquistes se digieren en el tracto gastrointestinal, liberándose cuatro esporozoítos que invaden de forma activa las células intestinales, destruyéndolas, especialmente aquellas localizadas al final del intestino delgado. En esta localización, el parásito experimenta varios ciclos de multiplicación que conducen a la destrucción de un elevado número de células intestinales, lo que disminuye notablemente la superficie de absorción.
Además, las células destruidas se restituyen a base de células inmaduras con menor capacidad digestiva y de absorción. Todas estas alteraciones desencadenan un proceso de malabsorción que origina la diarrea. La última fase de multiplicación del parásito dará lugar al ooquiste. La mayoría de los ooquistes poseen una pared gruesa y son eliminados al exterior con las heces, lo que les permite infectar a otros animales. Por el contrario, un menor porcentaje de ooquistes, cercano al 20 %, desarrollan una única membrana que se rompe con facilidad en la luz intestinal liberando otros cuatro esporozoítos, lo que da comienzo de nuevo al ciclo y son responsables de la autoinfección.
Se ha comprobado que, cuando las condiciones son óptimas, con temperaturas moderadas cercanas a los 15 °C, el parásito se puede mantener infectante durante largos periodos de tiempo, que pueden superar el año
Este ciclo, aparentemente sencillo, presenta diferentes particularidades que hacen que C. parvum sea un parásito extremadamente frecuente en las granjas de ganado vacuno, y muy complicado de eliminar de las instalaciones. Entre ellas se encuentran:
a) C. parvum es un parásito que puede completar su ciclo en numerosas especies de animales. Así, se ha comprobado que puede afectar hasta a 155 mamíferos diferentes (Fayer, 2004). Esto facilita la ingestión de los ooquistes por un animal, así como la multiplicación del parásito, lo que finalmente propiciará una mayor contaminación ambiental, incrementando la presión de infección.
b) Una de las claves de la supervivencia de este parásito es su localización en la célula intestinal: C. parvum se encuentra dentro de la célula, pero separado del contenido celular por una organela de alimentación que posee una función clave: regula el transporte de ciertas moléculas al interior del parásito. En este sentido, se ha demostrado que algunos fármacos con gran eficacia frente a otros protozoos intestinales, como los coccidios, no eliminan a C. parvum pues no son capaces de atravesar esta barrera y, por tanto, de alcanzar el interior del parásito (Barta & Thompson, 2006). Todo ello explica por qué se dispone de muy pocos fármacos con actividad frente a este protozoo, lo que dificulta su control y prevención.
c) C. parvum se disemina muy rápidamente entre terneros debido a su elevado potencial reproductor: un animal parasitado elimina con las heces un número elevadísimo de ooquistes de pared gruesa, lo que se traduce en una gran contaminación ambiental, que incrementa notablemente la presión de infección. Se ha descrito que un único ternero con diarrea puede eliminar entre un millón y 10 millones de ooquistes por gramo de heces (Nydam et al., 2001). Así, se ha estimado que, durante el periodo en que el animal excreta ooquistes, la eliminación total puede alcanzar los 40.000 millones. Pondremos algunos ejemplos que permitirán comprender mejor la elevadísima contaminación ambiental: el número de ooquistes excretados por un animal infectado es 4.000 veces superior a todos los ladrillos empleados en la contrucción del Empire State Building y 10 veces superior a los empleados en la Gran Muralla China.
d) Además, los ooquistes de pared gruesa eliminados poseen una elevada resistencia ambiental. Así, se ha comprobado que, cuando las condiciones son óptimas, con temperaturas moderadas cercanas a los 15°C, el parásito se puede mantener infectante durante largos periodos de tiempo, que pueden superar el año. También se mantienen viables tras exponerse a la acción de la mayoría de los desinfectantes, resistiendo la acción de la lejía y la cloración, por ejemplo. Se ha comprobado que los productos a base de peróxido de hidrógeno y compuestos de amonio cuaternario son especialmente eficaces (Quilez et al., 2005). Hay estudios que también señalan la cal viva como eficaz para inactivar los ooquistes (Björkman et al., 2018). También se puede recurrir a métodos físicos como la desecación, radiación solar, compostaje, etc., que comprometen la viabilidad de los ooquistes en el medio.
e) Los ooquistes que se excretan con las heces ya son directamente infectantes, por lo que pueden constituir la fuente de infección para otros animales justo tras su eliminación en las heces.
f) Finalmente, y como se comentó antes, tras la última fase de multiplicación del protozoo se forman también ooquistes de pared fina, cuya membrana se rompe con facilidad en la luz intestinal liberando los esporozoítos, lo que da lugar a la autoinfección.
Uno de los principales factores de riesgo para que un ternero se infecte por C. Parvum, es estar en contacto con otro ternero que sufra una diarrea por criptosporidios, debido a la alta eliminación de ooquistes y a la baja dosis infectante
Por lo tanto, en ausencia de una respuesta inmunitaria protectora, este protozoo puede mantenerse en un hospedador sin la necesidad de ingerir nuevos ooquistes. En consecuencia, la dosis infectante media es muy pequeña, es decir, el número de ooquistes que un animal debe ingerir para desarrollar y mostrar un cuadro clínico es muy bajo. Así, se demostró experimentalmente que, tras la ingestión de únicamente 17 ooquistes, el 50% de los terneros mostraban diarrea y eliminaban ooquistes, y todos lo hicieron con 132 ooquistes (Zambriski et al., 2013).
Por último, debemos tomar en consideración que el desarrollo de C. parvum puede verse favorecido por la combinación con otros patógenos. Un estudio reciente realizado en Galicia demuestra que el 82,1% de los terneros con diarrea estaban infectados por más de un patógeno, hasta un máximo de siete diferentes (López-Novo, 2023). En el caso concreto de C. parvum, en el 95% de los casos se identificó junto con otros agentes, demostrándose una interacción sinérgica de C. parvum con otros patógenos entéricos, especialmente víricos, cuya acción inmunosupresora podría facilitar el desarrollo del ciclo interno del protozoo.
Autor

Carlos Carbonell

Pablo Díaz
DIAGNÓSTICO | PREVENCIÓN | SALUD | TERNERAS
Artículos relacionados

POR FAVOR, INDICA CUÁL ES TU PROFESIÓN
ARTÍCULOS MÁS LEÍDOS
Cómo se gestiona la recría en Granja Santa Teresa
Nos adentramos en la finca El Gróo
Conoce la importancia de estimar el tiempo del aborto
La importancia de la evaluación reproductiva del toro
Cómo prevenir la diarrea neonatal
CATEGORÍAS
ETIQUETAS
ABORTOS · ANTIBIÓTICOS · BIENESTAR · BVD · CALIDAD · CALOSTRO · COMPOSICIÓN · CORPORAL · CONDICIÓN CORPORAL · CONSEJOS · DATOS · DATOS ECONÓMICOS · DATOS PATOLÓGICOS · DATOS PRODUCTIVOS · DATOS REPRODUCTIVOS · DESAFÍO · DIAGNÓSTICO · ECOGRAFÍA · EFICIENCIA PRODUCTIVA · ENCALOSTRADO · EXTENSIVO · FUTURO · GANADERO · GRANJA · INGLÉS · INMUNOGLOBULINA · LECHE · LENGUA AZUL ·NEUMONÍA · PI · PREINSEMINACIÓN · PREVENCIÓN · RENTABILIDAD · SALUD · SEMEN · SERVICIO · SOSTENIBILIDAD · SRB · TERNERAS · TESTAJE · TESTIMONIO · TOMA DE DECISIONES · TORO · VACUNACIÓN · VACUNO · VETERINARIO · VIRUS · VOCABULARIO



